| |
| |
|
Newsletter della Società Italiana di
Allergologia, Asma ed Immunologia Clinica - N.19/2020
|
|
|
|
| |
Sviluppo di un vaccino contro il COVID-19:
il panorama mondiale
|
|
|
|
| |
The COVID-19 vaccine development landscape Thanh Le T, et al. Nature reviews drug discovery. April 2020
|
|
|
|
| |
|
Di Carmela Irene & Samine Jessica Isaac, University of Trento
|
|
|
|
| |
Sintesi dello studio:
“Olfactory and gustatory dysfunctions as a clinical presentation of mild to moderate forms of the coronavirus disease ( COVID-19): a multicenter European study”. Lichien JR , Chiesa Estomba CM, De Siati DR et al.
Eur Arch Otorhinolaryngol. 2020 Apr 6. doi: 10.1007/s00405-020-05965-1.
|
|
|
|
| |
La sequenza genetica del SARS-CoV-2, il coronavirus che causa la malattia COVID-19, è stata pubblicata l’11 gennaio 2020, scatenando, su scala globale, un’intensa attività di ricerca per lo sviluppo di un vaccino contro la malattia. L’enorme impatto umanitario ed economico della pandemia COVID-19 ha favorito la valutazione di piattaforme tecnologiche per vaccini di nuova generazione, attraverso nuovi paradigmi per accelerarne lo sviluppo. Il primo vaccino COVID-19 è entrato nella fase I di sperimentazione sull’uomo con una rapidità senza precedenti il 16 marzo 2020. Le fasi di sperimentazione clinica prima della approvazione di un medicinale sono tre. Per i vaccini di solito possono durare da 5 a 15 anni. La Coalizione per la Preparazione e l’Innovazione alle Epidemie (CEPI) sta lavorando da una parte con le autorità della salute e dall’altra con gli inventori di vaccini per sostenere lo sviluppo di vaccini contro il COVID-19. Per facilitare questo sforzo, la rivista scientifica Nature Drug Discovery ha creato, e aggiorna continuamente, un database che raccoglie tutte le attività in corso per lo sviluppo di un vaccino. Questo include tutti i programmi di sviluppo del vaccino riportati attraverso l’autorevole lista dell’OMS, insieme ad altri progetti identificati da fonti sia pubbliche che private. Questa visione d’insieme fornisce informazioni sulle caratteristiche chiave dell’R&D (Ricerca e Sviluppo) per il vaccino contro COVID-19 e serve come risorsa per il management del portfolio del CEPI.
|
|
|
|
| |
|
Programmi di Ricerca e Sviluppo in corso a livello mondiale per un vaccino COVID-19
|
|
|
|
| |
|
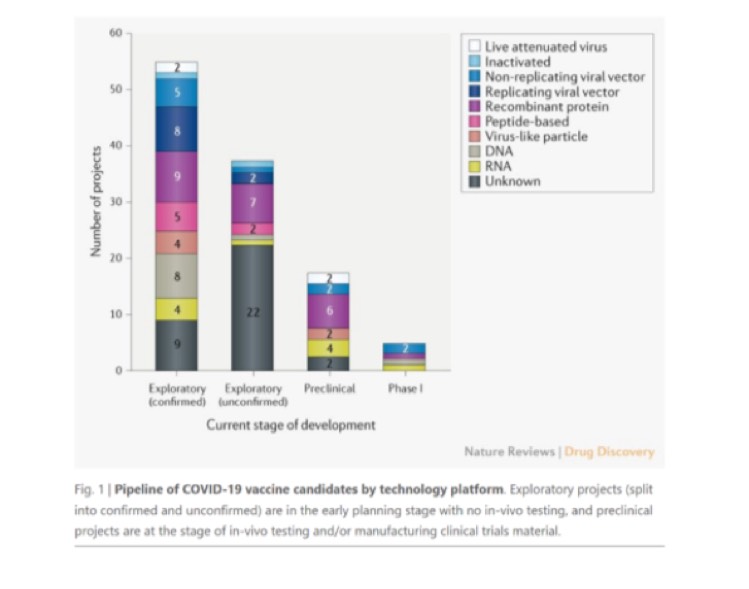
Alla data dell’8 di Aprile 2020, il panorama mondiale per lo sviluppo del vaccino COVID-19 include 115 possibili vaccini, di cui 78 confermati come progetti attivi e 37 non-confermati (il loro stato di sviluppo non può essere confermato con le informazioni pubblicamente disponibili).
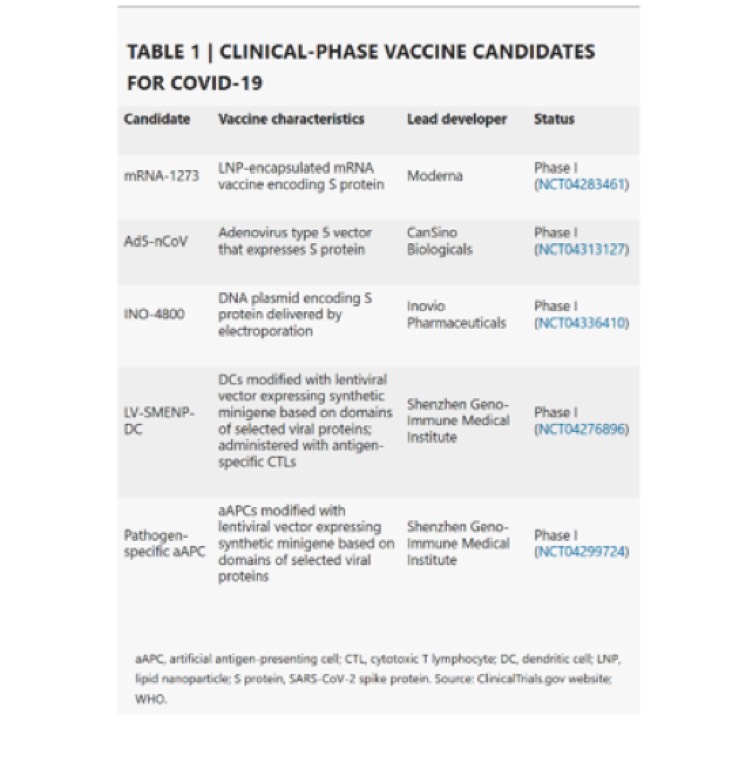
Dei 78 progetti confermati, 73 sono nello stadio di sviluppo preclinico. I 5 più avanzati sono arrivati negli ultimi giorni ad una prima fase di sperimentazione clinica nell’uomo. Essi sono:
1) un vaccino ad RNA incapsulato in nanoparticelle lipidiche di Moderna,
2) un vaccino che usa l’adenovirus Ade5 di CanSino Biologicals,
3) INO-4800 un vaccino basato su una molecola di DNA di Inovio,
4) e 5) due vaccini basati su cellule del sistema immunitario modificate con un lentivirus, di Shenzen Geno-Immune Medical Institute. Numerosi altri progetti hanno in programma di cominciare la sperimentazione nell’uomo nel 2020.
|
|
|
|
| |
|
Varietà delle piattaforme tecnologiche utilizzate
|
|
|
|
| |
Una caratteristica straordinaria in questa corsa mondiale per lo sviluppo del vaccino COVID-19 è la varietà di piattaforme tecnologiche utilizzate, esse includono acidi nucleici (DNA e RNA), particelle simili a virus, peptidi, vettori virali (replicativi e non replicativi), proteine ricombinanti, virus vivi attenuati e virus inattivati. Molte di queste piattaforme non sono ancora utilizzate per vaccini in commercio, ma attingendo all’esperienza in altri ambiti di ricerca, come ad esempio l’oncologia, incoraggiano gli inventori a sfruttare l’opportunità che questi nuovi approcci offrono per velocizzare lo sviluppo e la manifattura di un nuovo vaccino. È plausibile che diverse piattaforme possano essere più adatte a diversi gruppi della popolazione, come ad esempio anziani, bambini, gestanti o pazienti immuno-compromessi. Esaminiamo ad esempio i candidati già nella fase di sperimentazione nell’uomo (tabella 1). Le piattaforme che usano molecole di DNA e RNA offrono una grande flessibilità in termini di manipolazione degli antigeni (la parte del vaccino che mima il virus) e sono potenzialmente molto veloci da progettare e modificare. Infatti, gli inventori di Moderna, hanno cominciato i testi clinici con il loro vaccino ad RNA solo due mesi dopo l’identificazione della sequenza di RNA del virus. I vaccini che utilizzano invece i vettori virali hanno il vantaggio di avere un alto livello di espressione delle proteine e una stabilità a più lungo termine, oltre ad indurre una forte risposta immunitaria. Infine, i vaccini che utilizzano le proteine ricombinanti sono già in commercio per altre malattie, dunque questi candidati hanno il vantaggio di poter essere prodotti su larga scala, perché gli impianti di manifattura sono già in uso per altri vaccini. Per alcune piattaforme, l’uso di adiuvanti (insieme agli antigeni virali) potrebbe potenziarne l’immunogenicità, permettendo di usare dosi di vaccino più basse, e consentendo così la vaccinazione di un maggior numero di persone senza comprometterne l’efficacia. Fino ad ora, almeno 10 sviluppatori hanno indicato impianti per la produzione di vaccini e adiuvanti contro il COVID-19, e alcune grandi industrie farmaceutiche, produttrici di vaccini, come GSK, Seqirus e Dynavax, si sono impegnate a fornire i loro adiuvanti brevettati per l’uso nel nuovo vaccino, anche se fosse prodotto da altri. Le informazioni pubbliche sugli antigeni specifici SARS-CoV-2 usati nello sviluppo del vaccino sono limitate. La maggior parte dei candidati, per cui le informazioni sono pubbliche, puntano ad indurre anticorpi neutralizzanti contro la proteina di superfice virale spike (S) al fine di bloccarne l’ingresso nelle cellule attraverso il recettore cellulare ACE2. Tuttavia, non è chiaro se diverse forme o varianti della proteina S, usate nei diversi vaccini, siano simili le une alle altre, o quanto diverse forme della proteina possano essere legate all’epidemiologia della malattia. L’esperienza con lo sviluppo del vaccino contro la SARS suggerisce che è possibile potenziare l’effetto del vaccino combinando diversi antigeni. Questo tuttavia è ancora materia di discussione e potrebbe essere rilevante in una fase di perfezionamento del vaccino.
|
|
|
|
| |
|
Chi sono i soggetti coinvolti nello sviluppo del vaccino?
|
|
|
|
| |
|
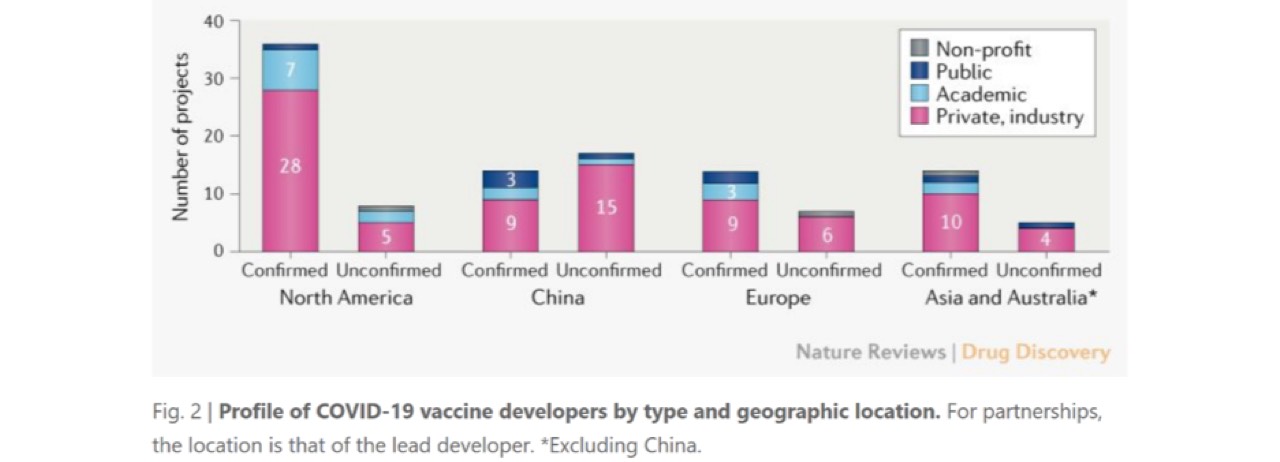
Dei progetti attivi, 56 (72%) appartengono ad industrie/privati, con i rimanenti 22 (28%) dei progetti condotti nelle Università, centri di ricerca pubblici and altre organizzazioni no profit.
|
|
|
|
| |
Sebbene un gran numero di grandi multinazionali produttrici di vaccini (Janssen, Sanofi, Pfizer, e GlaxoSmithKine) stiano attivamente lavorando sullo sviluppo del vaccino COVID-19, molti progetti coinvolgono piccole biotech e/o senza esperienza nella produzione su larga scala di vaccini. Per questo sarà importante assicurare una coordinazione tra manifattura del vaccino e capacità di fornitura per soddisfare la richiesta. La maggior parte dei progetti per lo sviluppo del vaccino sono in USA, con 36 (46%) dei progetti attivi confermati, 14 (18%) sono in Cina, 14 (18%) in Asia (esclusa la Cina) e Australia, 14 (18%) in Europa. Ulteriori progetti per lo sviluppo del vaccino sono stati riportati in Cina, e la CEPI è in contatto con il ministro della Scienza e della Tecnologia per confermare a che punto sono. I leader nello sviluppo di questo vaccino sono distribuiti in 19 paesi, complessivamente questi raccolgono più di ¾ della popolazione mondiale. Tuttavia, non ci sono al momento notizie sullo sviluppo di vaccini in Africa o America latina, anche se in queste regioni esistono sia la capacità di manifattura sia le strutture regolatorie. L’epidemiologia del COVID-19 potrebbe differire geograficamente, ed è probabile che un controllo effettivo della pandemia richiederà maggiore coinvolgimento e coordinazione con i paesi dell’emisfero meridionale nello sforzo di trovare il vaccino.
|
|
|
|
| |
La corsa globale allo sviluppo di un vaccino contro COVID-19 non ha precedenti in termini di velocità e portata. Il vaccino potrebbe essere disponibile agli inizi del 2021, ed usato nell’ambito di protocolli per le fasi più avanzate della sperimentazione clinica e non immediatamente come vaccino registrato e commercializzato. Perfino se comparato con i 5 anni per lo sviluppo del vaccino contro Ebola, questo rappresenterebbe un cambiamento sostanziale rispetto al tradizionale corso di sviluppo di un vaccino, il quale richiede mediamente 10 anni. Per tale ragione, necessiterà di nuovi paradigmi per lo sviluppo di vaccini che prevedono fasi di sviluppo parallele ed adattative, processi di regolazione innovativi, ed incremento della capacità di produzione. Gli standard industriali citano che per lo sviluppo tradizionale di un vaccino meno del 10% arriva ad essere registrato presso gli organismi regolatori Nazionali ed Internazionali. Le strategie innovative applicate allo sviluppo del vaccino del COVID-19 - il quale coinvolge un nuovo virus target e spesso una nuova piattaforma tecnologica e un nuovo paradigma di sviluppo - aumentano notevolmente il rischio associato al drug discovery/clinical trial e richiedono una valutazione attenta dell’efficacia e della sicurezza di ciascun passaggio. Per testare l’efficacia del vaccino, sono in corso di sviluppo nuovi modelli animali, questi includono topi, criceti e furetti transgenici che esprimono il recettore umano ACE2 e anche primati non umani. Laboratori con misure di contenimento biologico di livello 3 (uno dei più alti in termini di rischio e quindi anche sicurezza) sono necessari per gli studi con animali che prevedono infezioni con virus vivi, questo richiederà una coordinazione internazionale per assicurare che la capacità dei laboratori disponibili sia sufficiente. Infine, una forte coordinazione e cooperazione internazionale tra inventori del vaccino, organismi regolatori, decisori politici, strutture di sanità pubblica e governi sarà necessaria affinché i vaccini promettenti che superano le fasi più alte della sperimentazione possano essere prodotti in quantità sufficienti e distribuite in modo equo a tutte le regioni affette dalla pandemia, in particolare quelle con meno risorse. Il CEPI ha recentemente lanciato una campagna di raccolta fondi per supportare gli sforzi a livello globale per lo sviluppo del vaccino COVID-19 guidata da 3 imperativi: velocità, produzione e distribuzione su larga scala, e accesso globale.
|
|
|
|
|
|
|